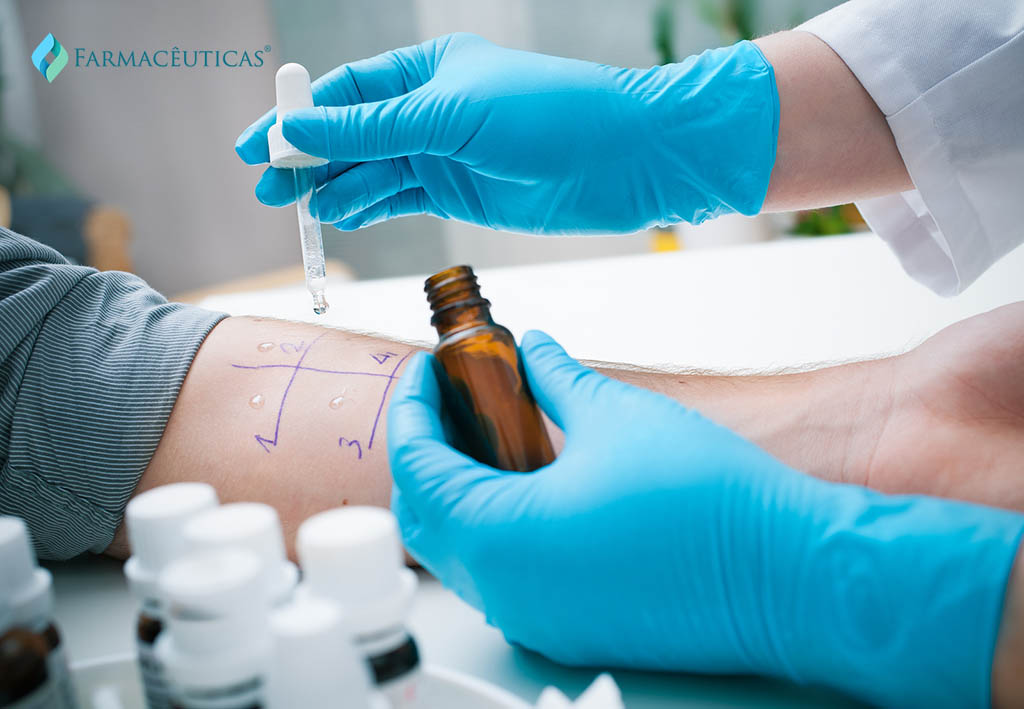
A Diretoria Colegiada da Anvisa aprovou um regulamento que atualiza as regras para o registro de medicamentos alergênicos. Estes produtos são vacinas para o tratamento de alergias e kits para o diagnóstico de alergias. A nova norma, que terá a forma de Resolução da Diretoria Colegiada (RDC), deverá ser publicada no Diário Oficial da União nos próximos dias.
[quote_center]O novo regulamento modernizará regras de registro de vacinas para o tratamento de alergias e kits para o diagnóstico de alergias.[/quote_center]
O texto aprovado na terça-feira, dia 7 de dezembro, atualiza a RDC 233/2005.
Registro de medicamentos alergênicos
As principais inovações da Norma para registro de medicamentos alergênicos são:
- Introdução do conceito de grupos homólogos, em substituição ao termo “família” de alérgenos, para o agrupamento de alérgenos semelhantes;
- Inclusão de demanda por adequada caracterização dos produtos alergênicos fabricados;
- Inclusão de demanda por melhor especificação do controle de qualidade a ser realizado nesses produtos;
- Demanda pela comprovação de eficácia e segurança clínicas, considerada a variabilidade entre produtos de diferentes fabricantes.
O que são alergênicos?
Produtos alergênicos são produtos biológicos utilizados para o diagnóstico, a prevenção ou o tratamento de alergias, por meio de imunoterapia por dessensibilização ou hipossensibilização. Os mecanismos de imunoterapia são bastante complexos e podem diferir de acordo com o alérgeno sensibilizador, se venenos, ou alérgenos inalados, bem como com a via de imunização.
Produtos alergênicos são derivados de várias fontes de alérgenos, como pólen, ácaros, substâncias alimentícias e fungos, os quais podem desencadear reação de hipersensibilidade.
A composição de extratos alergênicos varia conforme a fonte, processo de fabricação e condições de armazenamento. Tais fontes possuem quantidades não homogêneas de alérgenos, de modo que o processo de fabricação de extratos alergênicos é variável, devendo ser controlado e regulado para que o produto final seja eficaz e seguro.
Fonte
Anvisa